MADDENİN HALLERİ
Maddeler içinde bulundukları ortam koşullarına bağlı olarak katı, sıvı ve gaz olmak üzere üç halde bulunurlar.
Maddenin katı hali ve özellikleri:
- Belli bir şekilleri vardır
- Maddenin en düzenli halidir.
- Sıkıştırılamazlar
- Enerjileri azdır
- Atomlar sadece titreşim hareketi yapabilir
- Katı maddeler ısı alarak sıvı faza geçebilir
- Genleşme katsayısı ayırt edici özelliktir
- Kalem, kağıt, ağaç, ev, maddenin katı haline örnektir.
- Belirli bir şekilleri yoktur bulundukları kabın şeklini alırlar
- Maddenin sıvı hali katı haline göre daha düzensizdir
- Sıkıştırılamazlar
- Enerjileri maddenin katı haline göre daha fazladır
- Ötelenme dönme titreşim hareketi yaparlar
- Tanecikler arasında azda olsa çekim kuvveti vardır
- Sıcaklıkla genleşme kat sayısı ayırt edici özelliktir.
- Su, süt, zeytin yağı,, limonata, maddenin sıvı haline örnektir.
Maddenin gaz hali ve özellikleri;
- Maddenin en düzensiz halidir
- Enerjiisi katı ve sıvıya göre en yüksektir
- Tanecikler arasında boşluk en fazladır
- Belirli bir hacimleri yoktur sıkıştırılabilirler
- Gazlar birbirleriyle her oranda birleşerek homojen karışım oluştururlar
- Avagadro yasasına göre aynı sıcaklık ve basınç altında bulunan tüm gazların hacimleri eşittir.
- Bütün gazlar için genleşme katsayısı eşit olup 1/273 tür. Dolayısıyla gazlar için genleşme katsayısı ayırt edici özellik değildir.
- Hava,oksijen, duman, doğal gaz, azot karbondioksit maddenin gaz haline örnek verilebilir.
MADDENİN ÖZELLİKLERİ
Maddenin ortak özellikleri;
- Maddenin boşluklu ve tanecikli yapısı: Maddeyi atom, iyon ve molekül şeklindeki tanecikler oluşturur. Tüm maddeler taneciklerden oluşur ve tanecikler arasında boşluklar bulunur.
NOT:
Atom: Elementlerin özelliklerini taşıyan en küçük yapıtaşıdır. Atom proton, nötron, elektrondan oluşur.
Molekül: Birden fazla atomun bir araya gelerek oluşturduğu taneciklere molekül denir. O2, O3, H2O, CO2 örnek verilebilir.
İyon: Atom yada atom gruplarının elektron yüklenmiş haline iyon denir.
- Kütle: Madde miktarını belirten niceliktir. Eşit kollu terazi ile ölçülür . Birimi; miligram(mg), gram(g), kilogram(kg) ve ton olabilir. Kütle sıcaklık ve basınç değişikliklerinden etkilenmez .
- Ağırlık: Yer kürenin cisimlere uyguladığı çekim kuvvetine ağırlık denir. Ağırlık(G) kütle(m) ile yer çekimi ivmesinin(g) çarpımına eşittir. (G=mg)
NOT: Yer çekimi her yerde aynı değildir. ekvatordan kutuplara doğru gidildikçe yer çekimi ivmesi artar. dolayısıyla kutuplara gidildikçe cismin ağırlığı artar.
- Hacim: Maddenin boşlukta kapladığı yere hacim denir. Hacim sıcaklık ve basınca bağlı olarak değişir. Maddenin hallerine göre farklı hacim ölçüm yöntemi kullanılır.
- Eylemsizlik: Maddenin bulunduğu konumu koruma isteğidir. Eylemsizlik madde miktarına bağlı olarak değişir.
- Elektrikli yapıda olma: Maddenin içerisinde pozitif yüklü proton, negatif yüklü elektron ve yüksüz nötronun bulunmasıdır.
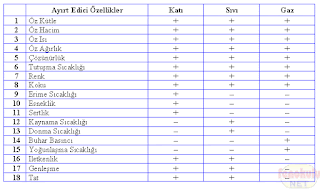
Maddenin ayırt edici özellikleri;
- Özkütle(Yoğunluk): Maddenin birim hacminin kütlesine öz kütle denir. (d=m/V) Formülü ile hesaplanır birimi g/cm^3 veya g/mL dir.Sabit sıcaklık ve basınçta tüm maddelerin öz kütleleri farklıdır. Bazı maddelerin öz kütle değerleri aşağıda verilmiştir.
- Altın: 19,30 g/cm3
- Su: 1g/cm3
- Benzin 0,879g/cm3
- Etil alkol :0,780g/cm3
- Zeytin yağı: 0,910g/cm3
- Genleşme katsayısı:Bir maddenin belli sıcaklık artışındaki büyüme miktarıdır. Genleşme katsayısı katı ve sıvılar için ayırt edici özelliktir. Bazı maddeler için genleşme katsayısı aşağıda gösterilmiştir.
katı madde,
Alüminyum ............ 69*10^-6
Bakır ............. 50*10^-6
çelik ............. 39*10^-6
cam ............... 27*10^-6
sıvı madde,
su ................ 0,21*10^-3
Alkol ................ 1,2*10^-3
civa ............... 0,18*10^-3
gliserin .............. 0,51*10^-3 - Esneklik katsayısı: Katı maddenin sertliğini ölçmek için kullanılan katsayı olup katı maddeler için ayırt edici özelliktir.
- İletkenlik: İletkenlik katı ve sıvılar için ayırt edici özellik iken gazlar için ayırt edici değildir.
- Erime noktası: Saf bir maddenin dışarıdan ısı alarak katı halden sıvı hale geçtiği sıcaklığa erime noktası denir. Erime noktası katı maddeler için ayırt edici özelliktir. Saf katıların erime noktaları dış basınç arttıkça artar. Fakat buzun istisna olarak dış basınç arttıkça erime noktası azalır. Bazı maddeler için erime noktaları aşağıda verilmiştir.
Hidrojen -259 C
Oksijen -219 C
Civa -38,8
Su 0 C
Gümüş 960 C
Altın 1063 C
Bakır 1087 C
- Donma noktası: Sıvı haldeki saf bir maddenin dışarıya ısı vererek katı hale geçmesine donma denir. Donma olayının gerçekleştiği sıcaklığa donma noktası denir. Saf maddelerin erime noktaları donma noktalarına eşittir.
- Kaynama noktası: Saf bir sıvının sabit basınç altında kaynamaya başladığı sıcaklığa kaynama noktası denir. Kaynama olayı sıvının buhar basıncının dış basınca eşit olduğu anda gerçekleşir. Kaynama sıcaklığı üzerinde sıvının cinsi, ortam basıncı ve safsızlıklar etkilidir.
- Öz ısı: Bir gram saf maddenin sıcaklığını bir derece arttırmak için gerekli ısı miktarına öz ısı denir.
- Buharlaşma ısısı: Kaynama sıcaklığındaki saf sıvının buhar fazına geçmesi için gerekli ısı miktarına buharlaşma ısısı denir.
- Yoğuşma ısısı: Yoğuşma sıcaklığındaki 1 gram saf gazın sıvı faza geçmesi sırasında dışarıya saldığı ısı miktarına yoğuşma ısısı denir.
- Donma ısısı: Bir gram saf sıvının donması sırasında çevreye saldığı ısı miktarına donma ısısı denir.
- Erime ısısı: Bir gram saf katının sıvı hale geçmesi için gerekli ısı miktarına erime ısısı denir.
Maddenin özellikleri fiziksel özellikler ve kimyasal özellikler olmak üzere ikiye ayrılır.
Fiziksel özellikler ve değişimler
Bir maddenin kimyasal bileşimini değiştirmeyen özelliklere fiziksel özellik denir. Maddenin kimyasal yapısını değiştirmeyen değişimlere ise fiziksel değişim denir.
Bir madde için renk, şekil, hacim,kırılganlık gibi özellikler fiziksel özellik iken maddenin hal değişimi, küçük parçalara bölünmesi, şeklinin değişmesi fiziksel değişimdir.
fiziksel değişime bazı örnekler aşağıda verilmiştir;
buzun erimesi
kağıdın buruşturulması ve yırtılması

Cam bardağın kırılması
Kimyasal özellikler ve değişimler
Bir maddenin çeşitli ortamlarda bileşimini değiştiren özelliklere kimyasal özellik denir. bir yada daha fazla maddenin farklı bileşimdeki maddeye dönüşmesine kimyasal değişme denir. Bir tahtanın yanabilmesi kimyasal özellik iken yanan tahta parçasının küle dönüşmesi kimyasal değişmedir.
Kimyasal değişime bazı örnekler aşağıda verilmiştir;
Asidin bazla nötürleşmesi
Zeytin yağından sabun eldesi
Etin kokuşması
Ekmeğin pişirilmesi
yumurtanın pişmesi,
Ekmeğin küflenmesi,
Mumun yanması
suyun elektrolizi
Demirin paslanması
Muzun çürümesi
Kağıdın yanması
Havai fişek patlaması